Abgeschlossen: Molecular Interaction Engineering (Syncasc)
- Ansprechperson:
- Förderung:
Nächste Generation biotechnologischer Verfahren (BMBF)
- Projektbeteiligte:
FZ Jülich/ IBG 1, KIT/ IFG, KIT/ IMT, KIT/ IBLT MAB, KIT/ TVT-TFT
- Starttermin:
01.01.2013
- Endtermin:
31.12.2018
Am Projekt mitwirkende wissenschaftliche Mitarbeiter
Teilprojekt "Synthetische Reaktionskaskaden" (SynCasc)
Projektbeschreibung: http://www.forschung-mie.de
Ihre Selektivität und die milden Reaktionsbedingungen machen Biokatalysatoren zu gefragten Katalysatoren chiraler Feinchemikalien insbesondere für die Pharmaindustrie. Durch die Kopplung von natürlich vorkommenden Enzymen aus unterschiedlichen Mikroorganismen mit maßgeschneiderten synthetischen Biokatalysatoren können auch in der Natur nicht vorkommende Verbindungen unter technischen Umgebungsbedingungen biobasiert hergestellt werden. Mit Enzymkaskaden lassen sich auf dieser Basis neue Synthesewege erschließen und klassische chemische Synthesen auf einer nachhaltigen Grundlage ersetzen:
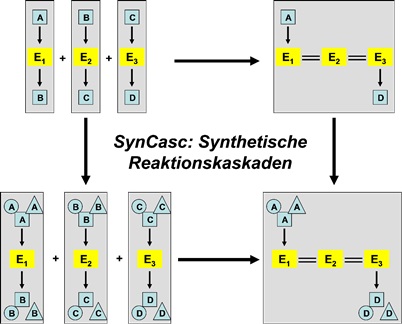
Im Rahmen der Projekte SC-1 und SC-2 werden am KIT und FZJ unterschiedliche enzymatische Verfahren zur Synthese nicht-kanonischer Aminosäuren sowie chiraler Alkohole mit pharmakologischer Relevanz etabliert.Hierbei liegt in der AG Syldatk/Rudat (SC-1) der Schwerpunkt auf der Produktion aromatischer chiraler α- und β-Ami¬no¬säu¬ren (e.g. β-Phenylalanin-Derivate), die bisher nur über chemoenzymatische Racematspaltung mit maximal 50% Ausbeute zugänglich sind. Hierzu werden zum einen Amidasen zur stereoselektiven Spaltung von Hydantoin-Derivaten verwendet, deren chemische oder enzymatische Racemisierung eine 100%ige Ausbeute ermöglicht. Alternativ sollen β-Ami¬no¬säu-ren durch Lipase-Transaminase-Kopp¬lung ausgehend von 3-Oxo-3-arylpropionsäure-Estern dargestellt werden, wobei ebenfalls eine 100%ige Reaktionsausbeute möglich ist.
Dabei sollen die modularen Enzymkaskaden zunächst als hybride zellfreie Systeme etabliert werden. Als Fernziel soll ein Reaktionskompartiment aus zwei bis drei gekoppelten maßgeschneiderten Enzymen bzw. chemo- und biokatalytischen funktionellen Komponenten zur Verfügung stehen, das durch erhöhte Substratvielfalt unterschiedliche Moleküle einer Verbindungsklasse über eine gesteuerte Mehrstufensynthese zum gewünschten Produkt umsetzen kann.
